몰 질량 분자량 차이: 화합물의 비밀 Revealed
원자량, 분자량, 몰(Mole)
Keywords searched by users: 몰 질량 분자량 차이 몰질량 계산, 분자량 단위, 몰 질량/원자량, 분자량 질량 관계, 분자량 구하기, 분자량 몰농도, 몰질량 단위, 분자량 몰수
몰 질량과 분자량의 심층 이해: 몰 질량 분자량 차이
한국어로 쓰여진 이 기사는 몰 질량과 분자량에 대한 심층적인 이해를 제공하며, 몰 질량 분자량의 차이를 자세히 설명합니다. 이 기사는 몰 질량과 분자량의 기본 개념부터 관련된 다양한 주제들에 대해 자세히 다룰 것입니다. 또한, 기사의 마지막에는 자주 묻는 질문(FAQs) 섹션이 포함되어 있습니다.
1. 몰 질량과 분자량의 기본 개념
물리학과 화학에서 몰 질량과 분자량은 물질의 양을 표현하는 데 중요한 역할을 합니다. 몰 질량은 한 몰의 물질에서의 질량을 의미하며, 이는 원자나 분자의 질량과 관련이 있습니다. 반면에 분자량은 분자가 가진 전체 질량을 나타냅니다.
2. 몰 질량과 분자량의 차이 이해하기
몰 질량과 분자량은 비슷한 개념으로 보일 수 있지만, 그 차이점은 각각의 측정 대상에 따라 다릅니다. 몰 질량은 동일한 물질의 한 몰에 대한 질량을 나타내는 반면, 분자량은 분자 단위의 질량을 의미합니다. 이 둘 간의 관계를 이해하면 화학 및 물리학에서 다양한 계산과 이론을 적용하는 데 도움이 됩니다.
3. 몰 질량의 정의와 계산 방법
한 몰의 물질에서의 몰 질량은 해당 물질의 원자 질량의 합으로 정의됩니다. 이것은 각각의 원자 질량을 모두 합산하여 얻을 수 있습니다. 수식적으로는 다음과 같습니다.
몰 질량(g/mol)=∑in원자 질량i
여기서 i는 물질에 포함된 원자의 개수이고, n은 총 원자의 수입니다.
4. 분자량의 정의와 계산 방법
분자량은 분자의 질량을 나타내는데, 이는 각각의 원자의 질량을 고려하여 계산됩니다. 분자량은 다음과 같이 표현됩니다.
분자량(g/mol)=∑jm원자 질량j
여기서 j는 분자에 포함된 각각의 원자를 나타내고, m은 총 원자의 수입니다.
5. 몰 질량과 분자량의 측정 단위
몰 질량과 분자량의 기본 단위는 g/mol입니다. 이 단위는 물질의 양을 표현하는 표준적인 방법으로 사용되며, 실험적인 측정 결과를 해석하는 데에도 중요한 역할을 합니다.
6. 몰 질량과 분자량의 활용 예시
몰 질량과 분자량은 다양한 화합물 및 물질에 대한 특성을 이해하고 예측하는 데 사용됩니다. 예를 들어, 화학 반응식에서 몰 질량과 분자량을 활용하여 반응 참여 물질 및 생성물의 양을 계산할 수 있습니다.
7. 몰 질량과 분자량의 화학 및 물리학적 응용
화학적인 관점에서 몰 질량과 분자량은 몰 개념을 기반으로 하는 다양한 화학 반응 및 반응 열역학에 중요한 역할을 합니다. 또한, 물리학에서는 분자량을 이용하여 다양한 물질의 물리적 특성을 연구하고 예측할 수 있습니다.
8. 몰 질량 분자량 차이의 실험적인 측정 방법
몰 질량과 분자량의 차이를 실험적으로 측정하는 데에는 여러 방법이 있습니다. 대표적으로는 질량 분석 장비를 사용하여 정확한 질량을 측정하거나, 분광학적인 방법을 활용하여 분자의 특성을 조사하는 등이 있습니다.
9. 몰 질량 분자량 차이 관련 자료 및 참고 자료
더 깊이 들어가기 위해서는 관련 자료 및 참고 자료를 살펴보는 것이 좋습니다. 아래는 몰 질량과 분자량에 관한 추가 정보를 얻을 수 있는 몇 가지 참고 자료입니다.
FAQs (자주 묻는 질문)
Q1: 몰 질량과 분자량이 동일한 경우가 있나요?
네, 어떤 경우에는 몰 질량과 분자량이 동일할 수 있습니다. 이는 물질이 하나의 원자로 이루어진 경우에 해당하며, 이러한 경우에는 해당 원자의 원자 질량이 그 물질의 몰 질량 및 분자량이 됩니다.
Q2: 몰 질량과 원자량의 차이는 무엇인가요?
몰 질량은 한 몰의 물질에서의 질량을 나타내는 것이고, 이는 해당 물질에 포함된 모든 원자의 질량을 합한 값입니다. 반면에 원자량은 하나의 원자의 질량을 나타냅니다.
Q3: 분자량을 구하는 방법은 무엇인가요?
분자량을 구하는 방법은 해당 분자에 포함된 모든 원자의 질량을 합산하는 것입니다. 분자식에서 각각의 원자 질량을 더하여 분자의 총 질량을 계산할 수 있습니다.
Q4: 몰 질량과 분자량의 활용 예시는 어떤 것이 있나요?
몰 질량과 분자량은 화합물의 반응량을 계산하거나 화학 반응식에서 물질의 양을 파악하는 데에 사용됩니다. 또한, 이러한 개념은 물리학적 특성을 연구하는 데에도 적용됩니다.
Q5: 몰 질량 분자량 차이를 실험적으로 어떻게 측정할 수 있나요?
몰 질량과 분자량의 차이를 실험적으로 측정하는 방법에는 여러 가지가 있습니다. 대표적으로는 정확한 질량 측정을 통한 방법이나 분광학적인 방법을 활용하는 방법이 있습니다.
결론
몰 질량과 분자량은 화학 및 물리학에서 중요한 개념으로, 이 두 가지를 제대로 이해하고 활용하는 것은 이 분야에서의 연구 및 실험을 수행하는 데에 필수적입니다. 몰 질량과 분자량의 차이를 깊이 이해함으로써 화학 및 물리학 관련 분야에서의 지식을 확장할 수 있을 것입니다.
Categories: 수집 51 몰 질량 분자량 차이

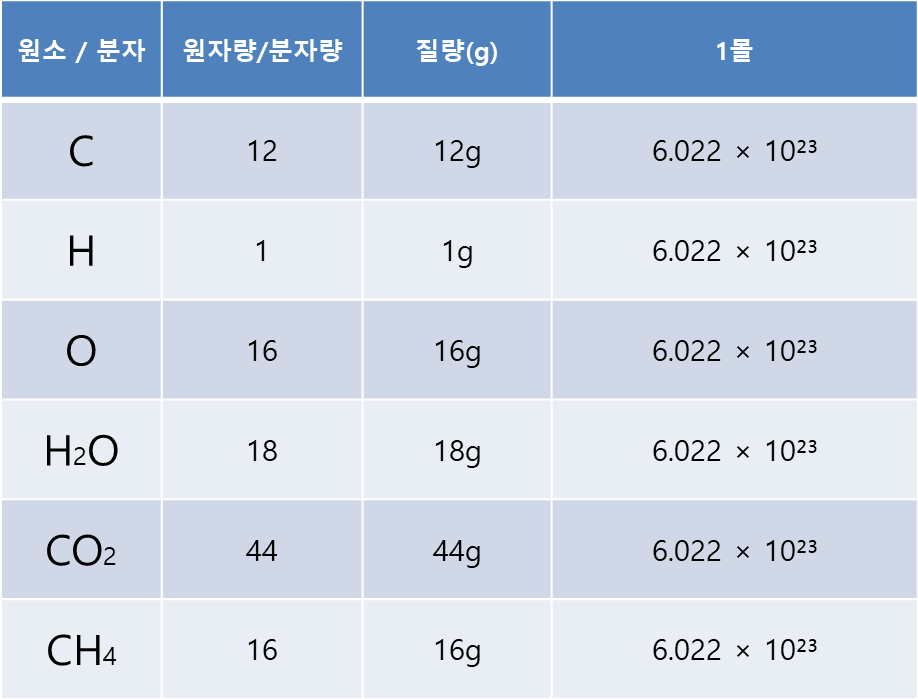
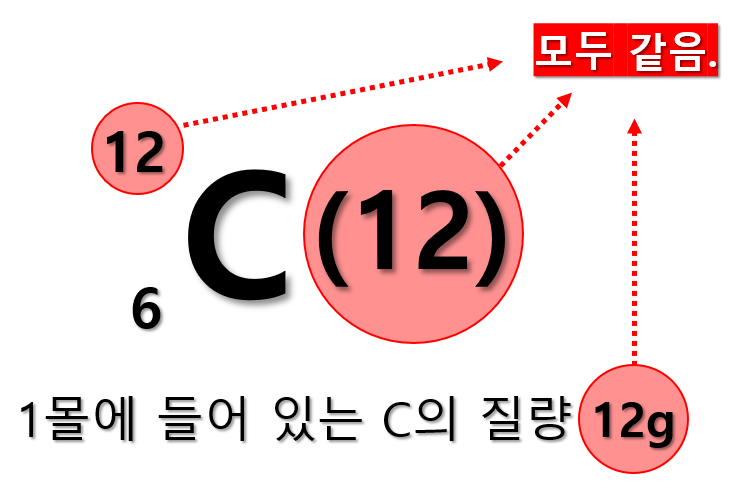
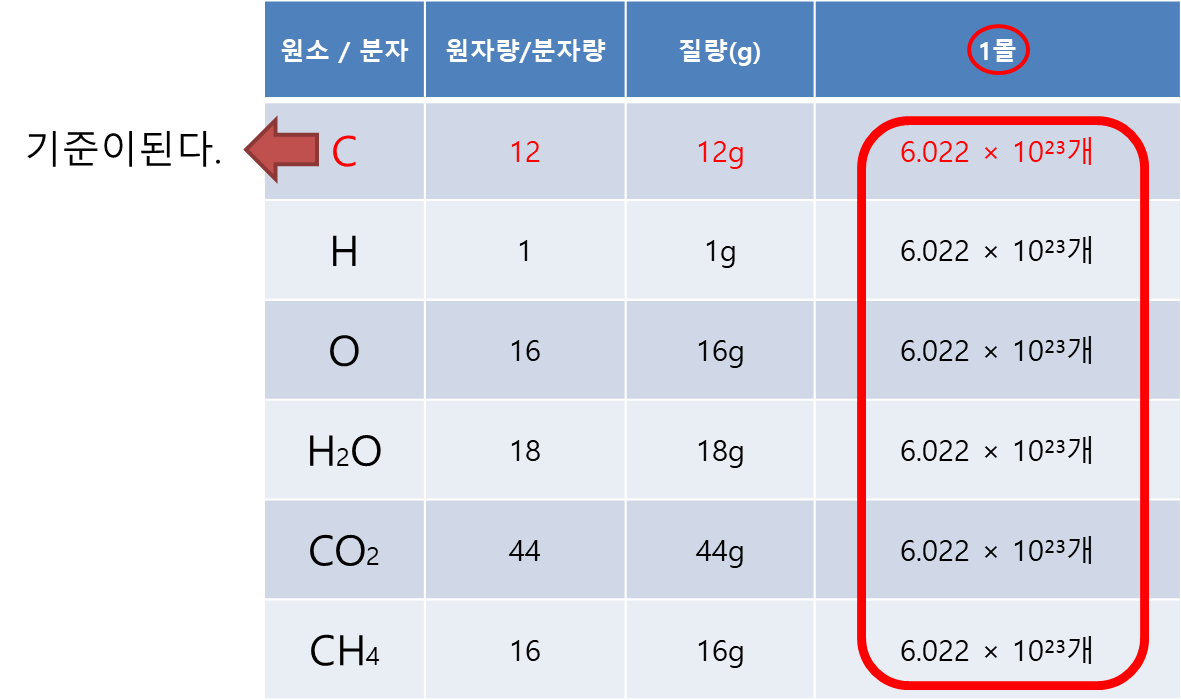
분자량은 상대질량이기 때문에 무차원량입니다. 즉, 단위는 없습니다. 즉, 분자량의 기준이나 생각은 원자량과 같습니다. 몰 질량은 어떤 물질 1 mol이 가지는 질량이며 단위도 존재합니다.몰(mole) – 몰은 정확히 12 g의 탄소-12 안에 들어있는 원자의 수와 같은 수 만큼의 개체로 이루어진 물질의 양. 일 몰(1 mole)은 (유효숫자 네 자리로) 6.022×1023 개체를 말한다.
1Mol 몇 G?
[몰(mole) – 몰은 정확히 12 g의 탄소-12 안에 들어있는 원자의 수와 같은 수 만큼의 개체로 이루어진 물질의 양을 나타내는 단위입니다. 탄소-12는 몰의 기준이 되며, 1 몰(1 mole)은 (유효숫자 네 자리로) 6.022×10^23 개체를 포함합니다. 이것은 Avogadro 수로 알려져 있으며, 이 수는 몰당 원자나 분자의 수를 나타내는 상수입니다. 따라서 몰은 물질의 양을 원자 또는 분자의 개수로 측정하며, 이를 통해 화학 반응식과 상호작용을 이해하는 데 도움이 됩니다.]
업데이트 33 몰 질량 분자량 차이



![문제풀이] 원자1개의 질량, 아보가드로수, 몰질량 - YouTube 문제풀이] 원자1개의 질량, 아보가드로수, 몰질량 - Youtube](https://i.ytimg.com/vi/U0cZdqiO2cM/maxresdefault.jpg)

![자연과학] 액체의 몰 질량 측정자연과학실험과제 자연과학] 액체의 몰 질량 측정자연과학실험과제](https://www.allreport.co.kr/View/[%EC%9E%90%EC%97%B0%EA%B3%BC%ED%95%99]%20%EC%95%A1%EC%B2%B4%EC%9D%98%20%EB%AA%B0%20%EC%A7%88%EB%9F%89%20%EC%B8%A1%EC%A0%95_hwp_03.gif)
![화학] 농도의 표현(퍼센트농도, 몰농도, 몰랄농도, 노르말농도, ppm) : 네이버 블로그 화학] 농도의 표현(퍼센트농도, 몰농도, 몰랄농도, 노르말농도, Ppm) : 네이버 블로그](https://mblogthumb-phinf.pstatic.net/MjAyMTAxMjBfMTMw/MDAxNjExMTUwOTA5OTcw.tjUnVQCUD6eCjx7ELEfGUGnfv8txz2O7GwLfp8Zhff4g.kOYs1e3X2CLXbhkj1Tp8RVKkxg5-es-bY1BAl9J59AMg.PNG.goodtime_92/image.png?type=w800)
![자연과학] 액체의 몰 질량 측정자연과학실험과제 자연과학] 액체의 몰 질량 측정자연과학실험과제](https://www.allreport.co.kr/View/[%EC%9E%90%EC%97%B0%EA%B3%BC%ED%95%99]%20%EC%95%A1%EC%B2%B4%EC%9D%98%20%EB%AA%B0%20%EC%A7%88%EB%9F%89%20%EC%B8%A1%EC%A0%95_hwp_02.gif)

![일반화학실험]액체의 몰질량 측정 레포트 일반화학실험]액체의 몰질량 측정 레포트](https://image4.happycampus.com/Production/thumb212/2015/04/05/data13181149-0001.jpg)
![자연과학]일반화학 - 몰 질량의 측정물리화학실험과제 자연과학]일반화학 - 몰 질량의 측정물리화학실험과제](https://www.allreport.co.kr/View/[%EC%9E%90%EC%97%B0%EA%B3%BC%ED%95%99]%EC%9D%BC%EB%B0%98%ED%99%94%ED%95%99%20-%20%EB%AA%B0%20%EC%A7%88%EB%9F%89%EC%9D%98%20%EC%B8%A1%EC%A0%95_hwp_01.gif)
See more here: future-user.com
Learn more about the topic 몰 질량 분자량 차이.